FDA 승인 받은 '레켐비' 이어 '도나네맙'이 최근 임상 효능 입증해
WHO, 향후 2050년 치매 환자수 1억만여 명 넘을 것으로 전망
국내 추정 치매환자는 2030년 136만 명 기록... 2050년 300만 명 전망
국내 제약·바이오 기업들도 알츠하이머 치료제 개발에 속도
식품의약품안전처, 치매치료제 제품화 규제 지원
맞춤형 상담, 글로벌 기준 우선 적용, 신속심사 등 제공하는 브리지 프로젝트 추진
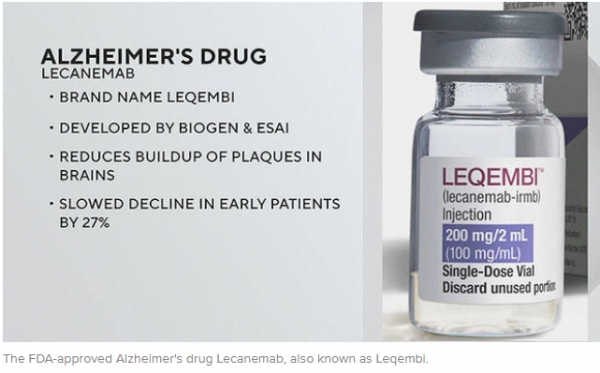
일본 에자이(Eisai)와 미국 바이오젠(Biogen)이 공동 개발하고 미국 식품의약국(FDA)의 승인을 받은 알츠하이머 치료제 '레켐비( lecanemab, 성분:레카네맙)'에 이어 세 번째 알츠하이머 신약이 될 것으로 기대받는 미국 제약사 '일라이 릴리'의 알츠하이머병 치료 물질 '도나네맙(donanemab)'이 최근 임상에서 효능을 입증함에 따라 치매 극복의 전환점이 도래했다는 기대가 커지고 있다.
고령화 사회 진입 속도가 빨라지면서 치매 환자 수도 급증하는 가운데 세계보건기구(WHO)는 향후 2050년에 치매 환자 수가 1억만여 명을 넘을 것으로 전망하고 있고, 미국 알츠하이머협회는 전 세계 알츠하이머 등 치매환자는 올해 7562만 명을 기록할 것으로 예상하고 있다.
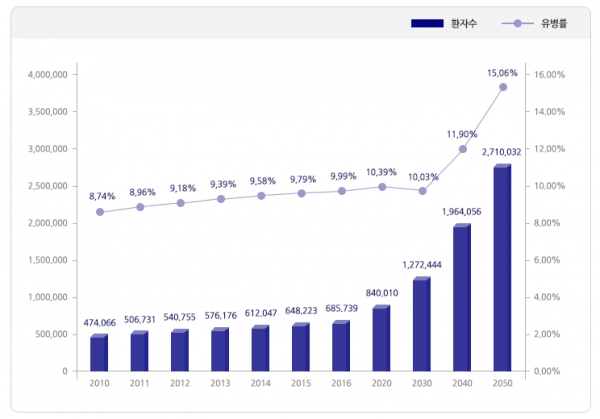
중앙치매센터에 따르면 2021년 국내 65세 이상 노인인구 중 추정 치매환자수는 88만6173명이었다. 치매유병률은 10.33%에 달했다. 이들을 관리하기 위한 치매관리비용은 총 18조7198억 원으로 추계됐다. 우리나라 추정 치매환자는 2030년 136만 명을 기록한 뒤 2050년 300만 명을 넘을 전망이다.
알츠하이머 치매 분야는 거대 시장이지만 획기적인 신약이 나오지 않아 질환을 근본적으로 치료할 수 있는 약은 아직 없었는데 최근 FDA의 승인을 받은 레켐비와 임상 효능을 입증했다는 도나네맙으로 치매 치료제 시장은 기대감이 커지고 있는 것이다.
국내 업계는 어떨까.
국내 제약·바이오 기업들도 알츠하이머 치료제 개발에 속도를 내고 있다. 알츠하이머병 치료제의 긍정적인 임상결과가 공개되고 있는 가운데, 국산 알츠하이머병 치료제의 가능성이 주목되고 있다.
업계에 따르면 국내에서 치매치료제 개발로 주목을 받고 있는 기업은 ▲아리바이오, ▲젬백스앤카엘, ▲디앤디파마텍, ▲차바이오텍, ▲엔케이맥스, ▲뉴로라이브, ▲샤페론, ▲이수앱지스, ▲메디프론, ▲브이티바이오, ▲지엔티파카 등이다.
아리바이오는 삼진제약과 라이선스 아웃(License-outㆍL/O) 계약을 맺고 이를 통해 AR1001의 미국 임상 3상 진행 중이며, 젬백스엔카엘의 'GV1001'의 경우 국내 임상 3상 승인을 받았으며, 삼성제약과 L/O 계약을 체결했다.
디앤디파마텍의 NLY01은 국내 임상 2상이 종료됐다. 차바이오텍의 줄기세포 치료제 'CB-AC-02'는 지금은 미진행 상태다. 엔케이맥스는 멕시코에서 'SNK01(이하 개발코드명)'의 임상 1상을 진행 중으로 알려졌고, 지난달에는 국내 임상 3상 신청을 완료했다고. 뉴로라이브는 알츠하이머 인지장애 치료제 후보물질 'NR-0701'을 개발하고 있다.
샤페론은 경증~중등도 알츠하이머병 환자를 치료하기 위한 후보물질 '누세린'을 개발 중이다. 이수앱지스의 'ISU203'는 현재 국내에서 비임상을 진행하고 있으며 올해 완료가 목표다. 비임상 종료 후 L/O를 통해 임상을 진행할 계획이라고 알려졌다.
메디프론도 알츠하이머병 치료제 후보물질 'MDR-0214'에 대한 국제 특허를 출원하고 개발 단계다. 브이티바이오의 VT301 국내 임상 1상은 완료됐으며, 미국(글로벌)은 임상 1상 시작 전 단계로 임상시험계획서(IND) 승인신청까지 마쳤다. 지엔티파마의 크리스데살라진은 국내 임상 2상 신청을 완료됐다.
식품의약품안전처, 치매치료제 제품화 규제 지원
7일 식약처는 정부가 지원하는 치매치료제 연구가 제품화로 이어질 수 있도록 지원하기 위해 치매극복연구개발사업단과 '치매치료제 국가 R&D 제품화 규제지원 간담회'를 열고, ▲식약처의 제품화 지원을 위한 상담체계 소개, ▲의약품 허가 절차 안내, ▲치매치료제 연구·개발 시 애로·건의 사항 청취, ▲치매치료제 개발을 지원하기 위한 관계부처의 규제지원 방안 논의, ▲과제별 1:1 맞춤형 상담 제공 등을 주요 내용으로 다룬다고 밝혔다.

국산 신기술이 혁신제품이 되어 세계시장을 선도할 수 있도록 국내 규제를 글로벌 스탠다드화 하는 동시에, R&D 코디, 맞춤형 상담(With-U), 규제 전문가 밀착 상담, 글로벌 기준 우선 적용, 신속심사 등을 제공하는 브리지(BRIDGE) 프로젝트를 추진하고 있다는 것.
식약처는 연구의 기획 단계부터 제품분류, 개발 전략, 임상시험계획 승인 등에 대해 사업단을 직접 찾아가 컨설팅하는 ‘맞춤형 상담(With-U)’을 적극 제공할 계획이라고 설명했다.
해외 승인된 치매 치료제의 국내 도입은 언제가 될까.
국내에서도 에자이가 식품의약품안전처에 레켐비의 품목허가를 신청했고, 이르면 내년 하반기 혹은 2025년 초 허가받는 것을 목표로 하고 있다. 도나네맙은 한국 도입 계획이 구체화되지 않았다. 국내 도입까지 시일이 걸릴 것으로 보이며, 미국 식품의약국(FDA)에는 승인을 신청한 상태다.
포인트경제 김지연 기자
- 붙이는 치매 치료제 '도네리온패취' 국내 출시
- 빛으로 치료 위치 표적하는 나노복합체로 치매 치료
- 7년 후의 파킨슨병을 예측하는 스마트 워치
- 대기오염이 치매 위험을 증가시킨다는 증거
- 붙이는 치매 치료제, '도네리온패치' 심포지엄 열린다
- 기억 장애 증상 전 알츠하이머 알아낼 혈액 검사?
- [펙트체크] 사회적 고립은 노인 치매 위험 높인다?
- 전신농포성 건선 치료 신약 '스페비고주', 국내 최초 허가
- '너의 기억을 지워줄게' ...줄기세포의 새로운 진화
- 20년 전에 알츠하이머 위험 예측하는 간단 테스트 고안..."5년 이내 사용 기대"
- 나주시, 치매 전수조사 실시…치매 환자 648명 발굴
- 커피 찌꺼기가 알츠하이머·파킨슨병을 예방한다?
- '보청기'가 치매를 예방한다?

