표적치료제 '다사티닙' - 세포 성장 관여하는 티로신 키나아제 역할 저해 (종양 세포 증식 억제)
다사티닙 장기복용 - 소변 내 단백질 수치 높아, 10%는 심각, 광범위한 신장 손상
임상 진료와 치료 기준 변화, 취약군 파악으로 대체 치료 계획 가능
백혈병에 일반적으로 사용되는 '다사티닙'이 신장 손상을 일으킬 수 있다는 새로운 연구 결과가 나왔다. 이 발견은 관련 질환의 임상 실습과 치료 기준에 변화를 가져오고 신약 개발에도 영향을 미칠 수 있다.
미국 마운트 시나이 의과대학이 주도한 이번 연구는 다사티닙을 복용하는 환자의 신장 손상 발생률을 확인하기 위한 다기관 임상 연구로 '미국신장학회 임상저널'(CJASN) 9월 호에 실렸다.
서울대학교 암병원의 약물정보에 따르면 스프라이셀(Sprycel)로 알려진 다사티닙(Dasatinib)은 표적 치료제 중에 '신호 전달 억제제'로 분류된다. 표적 치료는 정상 세포를 손상시키지 않으면서 종양 세포를 공격하는 치료를 뜻한다.
다사티닙은 세포 성장에 관여하는 티로신 키나아제 역할을 저해해서 종양 세포의 증식을 억제하는 효과가 있다. 주로 만성 골수성 백혈병이나 급성 림프모세포성 백혈병의 치료에 사용한다.
흔한 부작용으로는 일시적인 혈구 수 감소, 빈혈, 구역·설사, 피로감, 부종, 근육·뼈 통증, 수분 저류 등이 있다. 그 밖에도 관절통, 체중 변화, 폐렴, 가려움, 부정맥 등이 나타날 수 있다.
<의료진에게 긴급하게 알려야 하는 경우>
▲38℃ 이상의 고열과 오한 등 감염의 징후 ▲코·구강·질·항문에 15분 이상 지속되는 상당한 출혈 ▲몸이 붓거나 심장박동이 빠르고 호흡곤란 같은 알레르기 반응 징후▲검은색 대변, 혈뇨, 다량의 멍과 같은 출혈 징후
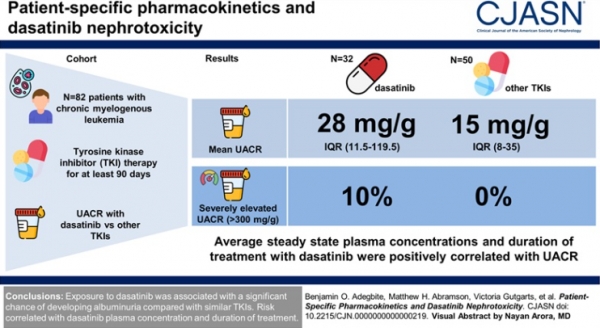
이 연구에는 만성 골수성 백혈병으로 장기간(최소 90일) 티로신 키나아제 억제제 치료를 받은 82명의 참가자가 참여했다. 32명은 다사티닙으로, 50명은 다른 티로신 키나아제 억제제(이마티닙 31명, 보수티닙 7명, 닐로티닙 10명, 포나티닙 2명)로 치료받았다.
단백뇨 측정 결과 다사티닙 그룹에서 높은 수준의 신장 손상이 확인되었으며 그중 10%는 심각한 수치를 보였다. 수치는 다사티닙 사용을 중단하면 감소했지만 완전히 사라지지는 않았다. 반대로 다사티닙을 사용하지 않은 그룹에서 중증의 단백뇨 사례는 없었다.
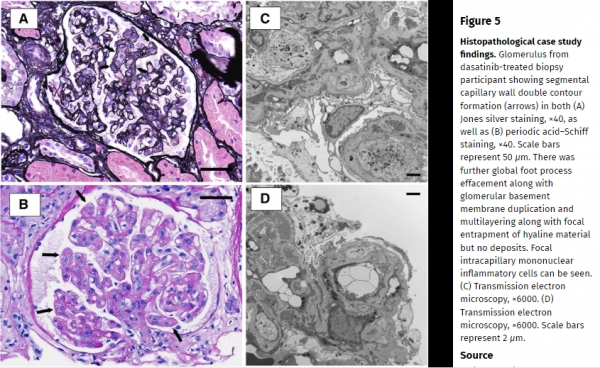
신장 조직 검사 결과 다사티닙 사용 그룹의 광범위한 신장 손상이 확인되었다.
이 결과를 바탕으로 다사티닙을 처방하는 전문의는 환자의 신장 기능이나 단백뇨를 모니터링하고 신장 전문의의 도움을 받도록 권고받을 수 있다. 특히 단백뇨가 심할 경우 치료법 변경도 고려될 것이다.
마운트 시나이 아이칸 의과대학 신장학 부교수이자 책임 연구자인 에브렌 U. 아젤로글루(Evren U. Azeloglu) 박사는 이러한 연구 결과가 현재의 임상 치료, 선별 가이드라인 및 부작용에 대한 미국식품의약국(FDA) 지침을 업데이트할 필요가 있다고 전했다.
또한 이 연구가 임상 진료에 큰 영향을 미쳐 표준 치료법을 바꾸고 연구 중인 약물에 대한 새로운 '블랙박스 경고'를 도입할 수 있을 것이라 예상했다.
블랙박스 또는 박스형 경고는 의료인이 처방할 때 신중을 기하도록 심각한 안전 위험을 수반하는 특정 약물에 FDA가 요구하는 경고문이다.
아젤로글루 박사는 이전 임상 시험에서 소변 내 단백질 수치가 높은 것으로 보고된 환자는 1% 미만이었음을 지적하며 "대규모 전향적 임상 연구를 통해 신장 손상에 더 취약한 환자 유형을 파악하고 대체 치료 전략을 세울 수 있다"라고 말했다.
포인트경제 박찬서 기자

