호중구, 혈액 내 세균 방어 첫번째 방어선
롤론티스, 환자 643명 대상 두 임상서 안전성·약효확인
국내 개발한 바이오신약 중 가장 큰 글로벌 성공 전망
8일 한미약품이 장기지속형 호중구감소증 치료 바이오신약 '롤론티스'의 국내 허가 신청서를 식품의약품안전처에 제출했다고 밝혔다.
이번 허가신청이 예정된 절차대로 심사될 경우, 롤론티스는 내년 상반기 국내에서 출시된다. 이미 FDA 시판허가 절차가 진행 중인 미국에서는 올해 하반기 출시가 예정돼 있다.
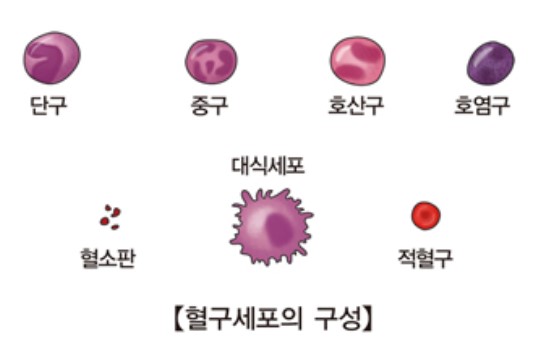
서울아산병원에 따르면 우리 몸의 백혈구 내에는 호중구, 호산구, 호염기구와 같은 과립구가 있는데 그중에 백혈구 내 차지하는 비율이 50~60%인 호중구의 수가 비정상적으로 감소된 것, 호중구의 수가 1500 이하로 감소된 경우를 호중구감소증이라고 한다.
호중구는 혈액 내 세균이나 박테리아가 우리 몸을 침범했을 경우 세균을 파괴하고 방어하는 첫 번째 방어선이므로 아주 중요한 역할을 담당하고 있다. 그래서 호중구감소증이 있는 환자는 의학적 조치가 없다면 쉽게 감염될 수 있고 생명을 위협당할 수도 있는 것이다.
이번 한미약품의 '롤론티스' 식약처 시판허가 신청은 파트너사 미국의 스펙트럼사가 주도한 2건의 글로벌 임상 3상 데이터를 토대로 제출됐다.
또한 골수억제성 항암화학요법으로 호중구감소증이 발생한 초기 유방암 환자 643명을 대상으로 진행된 두 임상에서 롤론티스의 안전성과 약효가 확인됐다.
롤론티스는 총 네 번의 치료 사이클 동안 경쟁약물 대비 DSN(Duration of Severe Neutropenia, 중증 호중구 감소증 발현기간)의 비열등성 및 우수한 상대적 위험 감소율 등이 입증됐다.
롤론티스는 한미약품이 개발하고 2012년 미국 제약기업 스펙트럼사에 라이선스 아웃한 바이오신약으로 바이오의약품의 약효과 투약 주기를 획기적으로 늘려주는 한미약품 독자 플랫폼 기술 '랩스커버리'가 적용됐다고 한다.
한미약품은 이 기술로 구현된 펩타이드 구조 자체의 신규성, 기존 약물 대비 적은 용량으로도 투여 횟수를 줄인 기술의 진보성을 토대로 식약처에 바이오신약 허가를 신청했다고 밝혔다.
한미약품 관계자는 "롤론티스는 한미약품의 독자기술 바이오신약들 중 처음으로 상용화되는 의미있는 제품으로 미국과 한국에서의 성공적 발매를 통해 글로벌에서 인정받도록 키워나가겠다"고 말했다.
한편 현재 국내 업체가 개발한 31개 신약 중 바이오신약은 3종뿐으로, 이 중 두 제품은 발매하지 않았거나 품목 취소됐고 나머지 한 품목은 연 매출 5억원대에 불과하다고 한다.
한미약품은 "한국의 호중구감소증 치료제 시장규모는 700여억원으로 롤론티스가 이 시장에 뛰어드는 한미의 첫번째 바이오신약이 되며, 내년 상반기 국내에서 출시되면 국내 업체가 개발해 시판한 바이오신약들 중 상업적 성공 가능성이 큰 제품이 될 전망"이라고 밝혔다.
포인트경제 박주현 기자

