오상헬스케어, 씨젠에 이어 국산 세번째
유전자 염기서열 증폭 진단하는 RT-PCR 검사법

오상헬스케어, 씨젠에 이어 국산 진단키트로는 세 번째로 에스디바이오센서의 코로나19 진단키트가 미국 식품의약국(FDA)의 긴급사용승인을 받았다.
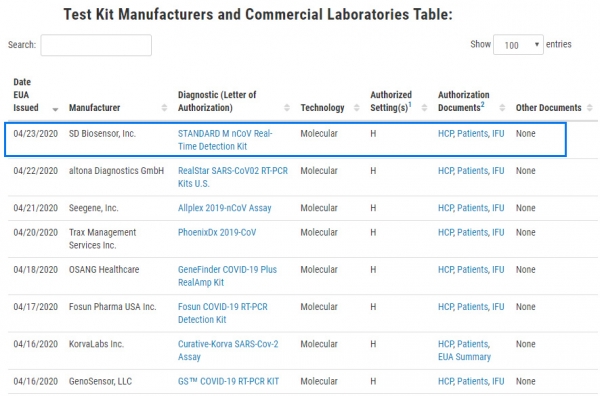
23일(현지시간) 미국 FDA는 에스디바이오센서의 ‘STANDARD M nCoV Real-Time Detection Kit’가 긴급사용승인을 받았다고 홈페이지에 공개했다.
FDA 체외진단 긴급사용승인(EUA) 제조업체 목록에 에스디바이오센서가 23일자로 표시되어 있는 것을 확인할 수 있었다. 목록에서 21일자에 씨젠의 진단키트가 18일자에는 오상헬스케어 진단키트가 확인되기도 했다.
앞서 에스디바이오센서는 올해 1월5일 코로나19 진단키트 개발에 착수해 해당 제품을 개발했다.
이 제품은 코로나19의 특정 유전자 염기서열을 증폭해 진단하는 RT-PCR 검사법이며 이후 2월27일 국내 긴급사용 승인을 먼저 받고 28일 수출용 허가를 획득했다.
에스디바이오센서는 이미 사스와 메르스를 신속 진단할 수 있는 키트를 개발한 체외진단업계 히든챔피언으로 알려졌다. 이어 인플루엔자, 지카 바이러스, 에볼라 바이러스 등에 대한 진단키트를 잇따라 개발하기도 했다.

이번 코로나19 진단키트는 CFX96과 ABI7500 등 2개 장비를 사용해 신속하고 간편한 검사 과정을 지닌다. ORF1ab, E gene을 이용한 검출로 높은 특이도·민감도가 장점이다.
에스디바이오센서는 미국을 포함해 60여개국에 코로나19 진단키트를 수출 중이라고 밝혔다.
포인트경제 박주현 기자
관련기사
박주현 기자
jhpark@pointe.co.kr

